El Ratón BALB/C: Un modelo animal para la investigación neurobiológica del ZIKA
Orlando Torres-Fernández1, Aura Caterine Rengifo1, Gerardo Santamaría1, Jorge Rivera1, Sheryll Corchuelo1, Julián Naizaque1, Alejandra Muñoz2
Grupo de Morfología Celular, Dirección de Investigación en Salud Pública, Instituto Nacional de Salud. 2- Bioterio, Instituto Nacional de Salud.
Resumen
El sistema nervioso central es el blanco principal de la infección con el virus del Zika, especialmente durante el desarrollo prenatal y postnatal temprano. Para estudiar los mecanismos celulares y moleculares que intervienen en la entrada del virus a las células nerviosas y los eventos patológicos que se desencadenan es necesario recurrir a modelos animales susceptibles a la infección. Nosotros logramos aislar y caracterizar un virus de Zika altamente neurotrópico cuando se inocula en ratones de la cepa Balb/c para desarrollar un modelo de infección con el cual hemos obtenido resultados importantes para contribuir al conocimiento de la neuropatogénesis del Zika.
Palabras clave: Virus del Zika, sistema nervioso, neurodesarrollo, ratones.
Summary
The central nervous system is the primary target of Zika virus infection, especially during prenatal and early postnatal development. To study the cellular and molecular mechanisms involved in the entry of the virus into nerve cells and the pathological events that are triggered, it is necessary to resort to animal models susceptible to infection. We managed to isolate and characterize a highly neurotropic Zika virus when inoculated into Balb/c strain mice to develop an infection model with which we have obtained important results to contribute to the understanding of Zika neuropathogenesis.
Keywords: Zika virus, nervous system, neurodevelopment, mice.
Origen y características del virus del Zika
En la selva del Zika cerca de Uganda (Kenia) se había instalado un laboratorio para el monitoreo de virus transmitidos por insectos vectores, en especial el de la fiebre amarilla; para ello se utilizaban monos del género Macacus. En suero obtenido de estos animales, en 1947, fue aislado por primera vez el que conocemos ahora como el virus del Zika (ZIKV) (1). Luego se estableció la asociación entre la infección con este virus y algunos signos y síntomas tales como fiebre, cefalea, artralgias, dolor muscular, conjuntivitis y erupciones cutáneas, todos ellos también presentes con otro tipo de infecciones transmitidas por insectos. Desde entonces se informaron casos esporádicos de Zika en diferentes países de África y Asia (2), pero fue hasta el año 2007 cuando se reportó la primera epidemia de Zika en Micronesia, territorio insular ubicado en Oceanía (3). En el 2013 el virus llegó a la Polinesia en donde se informó como novedad la asociación entre la infección con el ZIKV y el Síndrome de Guillain-Barré (4).
Desde la Polinesia el virus llegó hasta la isla de Pascua acercándose así a territorio americano, no obstante, debido a que la gran mayoría del territorio chileno no tiene las condiciones climáticas para albergar al vector Aedes aegypti, es poco probable que esa haya sido su ruta de entrada a territorio americano. La evidencia apunta a que el virus entró al Brasil en el año 2015 a través de migrantes procedentes del Caribe. De allí se dispersó en poco tiempo a Colombia y otros países en donde el A. aegypti se encuentra ampliamente distribuido en varias regiones por debajo de los 2000 m.s.n.m. (5,6).
El ZIKV es un arbovirus (virus transmitido por insectos), de la familia Flaviviridae, a la que pertenecen también otros arbovirus muy conocidos (dengue, fiebre amarilla, Chikungunya, el virus de la encefalitis equina y el virus del Nilo). El principal vector es el mosquito A aegypti que lo adquiere de la sangre de una persona infectada (2). El ZIKV está compuesto por una cadena de ARN de sentido positivo, es decir, que su genoma una vez que llega a la célula huésped tiene la capacidad de traducirse a proteína tal como sucede con otros flavivirus. El ZIKV codifica para tres proteínas estructurales (C, M y E), siete proteínas no-estructurales - NS1, NS2A, NS2B, NS3, NS4A, NS4B y NS5- y un péptido 2K. La proteína viral E es la que se une a los receptores de las células para permitir el ingreso del patógeno al citoplasma (7). El virus puede afectar diferentes órganos, pero su principal blanco es el sistema nervioso (8).
Neuropidemiología del ZIKV
La epidemia en Brasil llamó la atención debido al aumento significativo de casos de microcefalia en áreas en donde se diagnosticaron los primeros casos de Zika. Pronto se estableció la asociación epidemiológica entre la infección con ZIKV en mujeres gestantes y el nacimiento de niños con microcefalia y otros desordenes del desarrollo embrionario denominados en conjunto Síndrome de Zika Congénito (CZS) (9,10). Esto hizo que la Organización Mundial de la Salud declarara la alerta a nivel mundial y como consecuencia lógica despertó el interés de los investigadores (2). Con el fin de conocer los mecanismos moleculares y celulares que convirtieron al ZIKV en un patógeno neurotrópico e identificar las células blanco de su ataque, era indispensable acudir a la experimentación, por lo que resultó necesario desarrollar modelos de infección in vitro, así como modelos animales. Antes de la epidemia del 2015-2016 existían escasas referencias del uso de animales de laboratorio en el estudio del Zika. En 1952 se reportó por primera vez la infección intracerebral en ratones, además se encontró que el virus era altamente neurotrópico en el ratón con relación a otras especies tales como rata, conejo, conejillo de indias y monos (11). En 1971 se publicaron las primeras imágenes del virus observadas en el microscopio electrónico tomadas en tejido nervioso de ratones inoculados también por la ruta intracerebral (12).
Muy pronto a partir de la epidemia de 2015-2016 se estableció que las células más vulnerables a la infección en los modelos animales eran las células madre o células progenitoras neurales y se reportó que la proteína Mushashi-1 presente en estas células podría interactuar con las regiones no codificantes del genoma viral por ZIKV (13). Simultáneamente se encontró una mutación en una de las proteínas del virus determinante para que el ZIKV incrementara su infectividad en células progenitoras neurales (14); esto explicaba en parte de la mayor susceptibilidad a la neuroinfección durante el primer trimestre de gestación que tenía como consecuencia la microcefalia (15). La afinidad del virus por las células progenitoras neurales se corroboró cuando se inocularon ratones adultos y el virus se localizó principalmente en aquellas áreas en donde se conserva la neurogénesis, la zona subventricular y la zona subgranular en el giro dentado de la formación hipocampal (16). No obstante, también se estableció que la infección se puede dar en neuronas diferenciadas y células gliales en fases tempranas del neurodesarrollo postnatal en ratones (17).
Modelos animales para investigación del ZIKV
Puesto que el ZIKV generalmente ingresa al cuerpo humano a través de la picadura de mosquitos para entrar al torrente sanguíneo, era necesario desarrollar modelos animales en donde la infección fuera generada por vía periférica, esto significaba, inocularlos a través de la piel o intraperitonealmente. Se ensayó en el ratón por ser el animal de laboratorio más utilizado para la investigación con virus neurotrópicos. Sin embargo, los resultados no fueron los mejores debido a que esta especie es resistente a la infección con el ZIKV puesto que la proteína NS5 del ZIKV no es capaz de inhibir la respuesta del interferón como sí ocurre en el humano y otras especies susceptibles (18). Por esta razón, fue necesario recurrir a ratones modificados genéticamente (knock out para interferón) o inhibir la respuesta del interferón inoculando a los animales con un anticuerpo anti-INF antes de la inoculación con el ZIKV (19,20).
En nuestro grupo logramos, después de varios ensayos, obtener un modelo animal de infección con ZIKV utilizando ratones de la cepa Balb/c de un día de nacidos, sin que fuera necesario algún tratamiento especial de inmunosupresión (Figura 1). Estos animales se inocularon con un virus aislado de un paciente procedente de Villavicencio. A partir del día 6 postinoculación los animales manifestaron signos neurológicos tales como: hipersensibilidad al tacto, tremor, inestabilidad en la marcha, y finalmente parálisis de las extremidades posteriores, similar a lo que hemos observado en ratones inoculados con rabia, un virus estrictamente neurotrópico. Mediante RT-PCR, inmunohistoquímica e hibridación in situ se confirmó la infección con ZIKV y también se descartó la coinfección con dengue y Chikungunya (21,22,23,24). Con alguna frecuencia en los sueros de los pacientes puede hallarse evidencia de la presencia de dos o los tres virus debido a que comparten el mismo vector y condiciones ambientes. Nosotros establecimos un método de procesamiento y análisis molecular para identificar con certeza la presencia de cada uno de estos tres virus en una muestra para su diagnóstico diferencial (25).
Figura 1. Ratones Balb/c de 1 día de nacido (Izquierda) y ratones postnatales de 11 días (Derecha). Fotografías de Gerardo Santamaría (Grupo de Morfología Celular, INS).
Resultados de investigación obtenidos con el modelo animal Balb/c
Gracias a la obtención del modelo animal fue posible abordar el estudio de diferentes aspectos citomorfológicos y moleculares del efecto de la infección con ZIKV en el neurodesarrollo postnatal del ratón. Se considera que el encéfalo de un ratón recién nacido es equivalente en su estructura y función al de un encéfalo humano en desarrollo a partir del segundo trimestre de gestación (17,20). Por lo tanto, es posible extrapolar los resultados obtenidos en el modelo animal para interpretar los hallazgos de los efectos de la infección en el neurodesarrollo humano durante la segunda mitad del embarazo. Además de los signos neurológicos evidentes observados en los ratones y la demostración de la presencia del virus en su sistema nervioso, también se observaron calcificaciones en la corteza cerebral y el cerebelo. Estas se distinguieron a simple vista por su aspecto blancuzco lechoso por debajo de la superficie cortical y cerebelar, y se confirmó su naturaleza mediante la reacción histoquímica de Von Kossa (Figura 2). Este fenómeno ha sido también característico de los fetos humanos con microcefalia asociada al CZS (10).
Figura 2. Calcificación (masa blancuzca) en el hemisferio derecho de la corteza cerebral de un ratón inoculado con ZIKV y hemisferio izquierdo de la corteza cerebral de un ratón control. A la derecha un corte de cerebelo con calcificaciones (manchas negras) reveladas mediante la reacción histoquímica de Von Kossa (10X). Imágenes tomadas por Gerardo Santamaría.
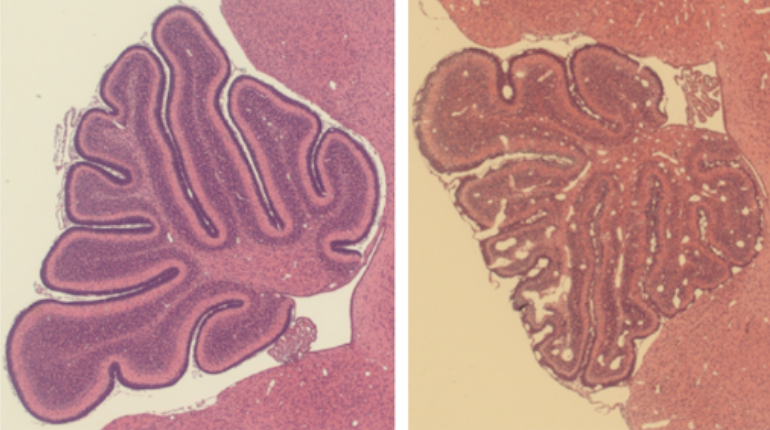
El estudio histológico reveló daño tisular, especialmente notorio en el cerebelo visto en un plano sagital (Figura 3). La atrofia o hipoplasia cerebelar se podría explicar en parte por la presencia en esta estructura de una capa exterior de células indiferenciadas que son más susceptibles a la infección mientras que en la corteza cerebral el número de células indiferenciadas en un ratón neonato es mucho menor. La hipoplasia cerebelar también ha sido documentada en el cerebelo de fetos y neonatos humanos afectados por el CZS (8,10).

Figura 3. Cortes sagitales de cerebelo coloreados con hematoxilina & eosina. A la izquierda cerebelo de ratón normal. A la derecha cerebelo de ratón inoculado con Zika que exhibe atrofia (hipoplasia) y extenso daño tisular (5X). Fotografías de Orlando Torres (Grupo de Morfología Celular, INS).
Si bien en la corteza cerebral de los ratones neonatos no se observó una pérdida notable en el número de neuronas en las imágenes histológicas convencionales, la inmunohistoquímica utilizando un anticuerpo anti-NeuN reveló pérdida acentuada de la inmunotinción (Figura 4). La proteína nuclear neuronal (NeuN) se encuentra casi exclusivamente en neuronas diferenciadas (26) y la pérdida de su expresión tisular generada por la infección podría ser un signo de neurodegeneración (27,28). También mediante la RT-qPCR se demostró la subregulación de esta proteína en extractos de corteza cerebral y cerebelo. Esto implica que, si bien el principal blanco del ZIKV son las células progenitoras neurales, también las neuronas maduras son afectadas. Estos hallazgos en el modelo animal de neurodesarrollo postnatal podrían estar relacionados con el hecho de que ya se ha demostrado también el efecto de la infección con ZIKV en el sistema nervioso del feto durante el embarazo avanzado y en los neonatos humanos (29).

Figura 4. Imágenes de fragmentos verticales de cortes coronales de corteza cerebral procesados para inmunohistoquímica de NeuN. Izquierda ratón control. Derecha ratón inoculado con ZIKV (40X). Nótese la pérdida de expresión de la proteína en las neuronas como resultado de la infección. Fotografías de Orlando Torres.
Mediante la técnica de Golgi-Cox se observó que la infección también afectó la morfología dendrítica de las neuronas en la corteza cerebral, el hipocampo y el cerebelo de los ratones (Figura 5). Este hallazgo tuvo soporte bioquímico y molecular puesto que la proteína asociada a microtúbulos MAP2, indispensable para dar estabilidad al citoesqueleto de las dendritas (30), mostró pérdida de expresión tisular evaluada por inmunohistoquímica. Así mismo se demostró disminución en la expresión de su ARN mensajero.

Figura 5. Neuronas de la capa piramidal del hipocampo en un ratón control (izquierda). En un ratón inoculado con ZIKV (derecha) no se observan neuronas con morfología normal en la misma zona (40X). Fotografías de Gerardo Santamaría.
Otros marcadores neuronales estudiados fueron las proteínas reguladoras de calcio intracelular: calbindina (CB), calretinina (CR) y parvoalbúmina (PV) (31). CB no reveló marcación en la corteza cerebral de los ratones, pero sí en las células de Purkinje del cerebelo. La infección con ZIKV generó pérdida en la expresión de esta proteína y permitió identificar también pérdida en el número de células de Purkinje. Las proteínas CR y PV aumentaron su expresión en la corteza cerebral de los ratones inoculados con ZIKV. Los cambios en la expresión de estas proteínas en los ratones infectados podrían estar relacionados con la formación de las calcificaciones.
En conclusión, en el Grupo de Morfología Celular del Instituto Nacional de Salud hemos logrado llevar a cabo un estudio para evaluar el efecto de la infección con virus del Zika en el sistema nervioso que requirió inicialmente aislar de un paciente una cepa del ZIKV con características altamente neurotrópicas. Esto permitió desarrollar nuestro propio modelo animal inmunocompetente para la investigación de esta patología viral. La investigación fue posible en gracias a la cofinanciación del proyecto “Estudio del efecto de la infección por virus Zika sobre la citomorfología, la neurobioquímica y el neurodesarrollo en modelos in vivo e in vitro. Financiación: Colciencias (Minciencias) Código: 210474455818. Contrato INS-Colciencias-Salutia 672 de 2017.
Referencias:
- Newman C, Friedrich TC, O’Connor DH. Macaque monkeys in Zika virus research: 1947-present. Curr Opin Virol. 2017;25: 34–40.
- Kindhauser MK, Allen T, Frank V, Santhana RS, Dye C. Zika: the origin and spread of a mosquito-borne virus. Bull World Health Organ. 2016;94(9):675-686C. doi: 10.2471/BLT.16.171082.
- Duffy MR, Chen TH, Hancock, Powers AM, Kool JL, Lanciotti RS, et al. Zika virus outbreak on Yap Island, Federated States of Micronesia. N Engl J Med 2009; 360: 2536-43.
- Cao-Lormeau VM, Blake A, Mons S, Lastère S, Roche C, Vanhomwegen J, et al. Guillaín-Barré Syndrome outbreak associated with Zika virus infection in French Poynesia: a case-control study. Lancet. 2016;387(10027):1531-39.
- Metsky HC, Matranga CB, Wohl S, Schaffner SF, Freije CA, Winnicki SM, et al. Zika virus evolution and spread in the Americas. Nature. 2017;546(7658):411-5.
- Tolosa N, Tinker SC, Pacheco O, Valencia D, Salas D, Tong VT, et al. Zika virus disease in children in Colombia, August 2015 to May 2016. Paediatr Perinat Epidemiol. 2017; 31: 537–45.
- Sirohi D, Chen Z, Sun L, Klose T, Pierson TC, Rossmann MG, Kuhn RJ. The 3.8Å resolution cryo-EM structure of Zika virus. Science. 2016;352(6284):467-70.
- Carod-Artal FJ. Epidemiología y complicaciones neurológicas de la infección por el virus Zika: un nuevo virus neurotropo emergente. Rev Neurol 2016; 62: 317-28.
- Brady OJ, Osgood-Zimmerman A, Kassebaum NJ, Ray SE, de Araújo VEM, da Nóbrega AA, et al. The association between Zika virus infection and microcephaly in Brazil 2015-2017: An observational analysis of over 4 million births. Observational Study. PLoS Med 2019; 5;16 (3): e1002755. doi: 10.1371/journal.pmed.1002755.
- Freitas DA, Souza-Santos R, Carvalho LMA, Barros WB, Neves LM, Brasil P, Wakimoto MD. Congenital Zika syndrome: A systematic review. PLoS ONE 2020;15(12): e0242367. https://doi.org/10.1371/journal.pone.0242367.
- Dick GW. Zika virus. II. Pathogenicity and physical properties. Trans R Soc Trop Med Hyg. 1952;46: 521–34.
- Bell TM, Field EJ, Narang HK. Zika virus infection of the central nervous system of mice. Arch Gesamte Virusforsch. 1971; 35:183-93.
- Chavali PL, Stojic L, Meredith LW, Joseph N, Nahorski MS, Sanford TJ, et al. Neurodevelopmental protein Musashi-1 interacts with the Zika genome and promotes viral replication. Science. 2017;357(6346):83-88.
- Yuan L, Huang XY, Liu ZY, Zhang F, Zhu XL, Yu JY, et al. A single mutation in the prM protein of Zika virus contributes to fetal microcephaly. Science. 2017;358(6365):933-6.
- Wen Z, Song H, Ming GL. How does Zika virus cause microcephaly? Genes Dev. 2017;31(9):849-61.
- Li H, Saucedo-Cuevas L, Regla-Nava JA, Chai G, Sheets N, Tang W., et al. Zika virus infects neural progenitors in the adult mouse brain and alters proliferation. Cell Stem Cell. 2016; 19:1-6.
- Van den Pol A, Mao G, Yang Y, Ornaghi S, Davis JN. Zika virus targeting in the developing brain. J Neurosci. 2017; 37(8):2161–75.
- Grant A, Ponia SS, Tripathi S, Balasubramaniam V, Miorin L, Sourisseau M, et al. Zika Virus Targets Human STAT2 to Inhibit Type I Interferon Signaling. Cell Host Microbe. 2016;19(6):882-90. doi: 10.1016/j.chom.2016.05.009.
- Bradley MP, Nagamine CM. Animal models of Zika virus. Comp Med. 2017;67:242-52.
- Narasimhan H, Chudnovets A, Burd I, Pekosz A, Klein SL. Animal models of congenital zika syndrome provide mechanistic insight into viral pathogenesis during pregnancy. PLoS Negl Trop Dis. 2020 Oct 22;14(10):e0008707. doi: 10.1371/journal.pntd.0008707.
- Torres-Fernández O, Rengifo-Castillo A, Álvarez-Díaz DA, Corchuelo S, Santamaría G, Monroy-Gómez J, et al. Obtención de un modelo animal para el estudio de la infección por el virus del Zika. Biomédica. 2017;37(3):2.
- Laiton-Donato K, Álvarez-Díaz DA, Rengifo AC, Torres-Fernández O, Usme-Ciro JA, Rivera JA, et al. Complete genome sequence of a Colombian Zika virus strain obtained from BALB/c mouse brain after Intraperitoneal Inoculation. Microbiol Resour Announc. 2019;8(46): e01719-18.
- Rivera J, Rengifo AC, Santamaría G, Corchuelo S, Álvarez-Díaz D, Torres-Fernández O, et al.Immunoreactivity of Zika virus infection in mouse retina. Biomédica. 2019; 39 (Supl. 2):8-10.
- Corchuelo S, Gómez CY, Rosales AA, Santamaria G, Rivera JA, Torres-Fernández O, Rengifo AC. CISH and IHC for the simultaneous detection of ZIKV RNA and antigens in formalin-fixed paraffin-embedded cell blocks and tissues Curr Protoc. 2021; 1(12):e319. doi: 10.1002/cpz1.319.
- Álvarez-Díaz DA, Valencia-Álvarez E, Rivera JA, Rengifo AC, Usme-Ciro JA, Torres-Fernández O, et al. An updated RT-qPCR assay for the simultaneous detection and quantification of chikungunya, dengue and zika viruses. Infect Genet Evol. 2021; 93:104967. doi: 10.1016/j.meegid.2021.104967.
- Guselnikova VV, Korzhevskiy DE. NeuN as neuronal nuclear antigen and neuron differentiaton marker. Acta Naturae. 2015; 7:42-7.
- Collombet JM, Masqueliez C, Four E, Burckhart MF, Bernabé D, Baubichon D, Lallement G. Early reduction of NeuN antigenicity induced by soman poisoning in mice can be used to predict delayed neuronal degeneration in the hippocampus. Neurosci Lett. 2006; 398:337-342.
- Lavezzi AM. A new theory to explain the underlying pathogenetic mechanism of sudden infant death syndrome. Front Neurol. 2015; 6:220. https://doi.org/10.3389/fneur.2015.00220
- Lebov J, Brown L, MacDonald P, Robertson K, McCarter-Bowman N., et al. Review: Evidence of neurological sequelae in children with acquired Zika virus infection. Pediatr. Neurol. 2018; 85: 16-20.
- Koleske AK. Molecular mechanisms of dendrite stability. Nat Rev Neurosci. 2013; 14(8):536-50. doi: 10.1038/nrn3486.
- Fairless R, Williams SK, Diem R. Calcium-Binding Proteins as Determinants of Central Nervous System Neuronal Vulnerability to Disease. Int J Mol Sci. 2019 30; 20(9):2146. doi: 10.3390/ijms20092146.













